Il cancro rappresenta una delle principali cause di morbilità e mortalità a livello globale, con un’incidenza in aumento prevista nei prossimi anni a causa dell’invecchiamento della popolazione. Questo scenario sottolinea la necessità di sviluppare strategie terapeutiche innovative, altamente tollerabili e con bassa tossicità per migliorare la qualità della vita dei pazienti. La nanomedicina emerge come una risposta promettente a questa esigenza, offrendo la possibilità di personalizzare i trattamenti in base alle caratteristiche genetiche e immunofenotipiche del tumore di ciascun paziente. Grazie all’uso delle nanotecnologie, è possibile garantire un rilascio mirato dei farmaci, migliorando l’efficacia del trattamento e riducendo gli effetti collaterali.
Cos’è la nanomedicina
La nanomedicina applica le nanotecnologie alla diagnosi e al trattamento delle malattie, utilizzando materiali su scala nanometrica per migliorare l’efficacia dei farmaci e ridurre gli effetti collaterali. In oncologia, le nanoparticelle permettono un rilascio mirato del farmaco alle cellule tumorali, aumentando l’efficacia e riducendo la tossicità. Oltre al cancro, trova applicazione in neurologia e cardiologia, ad esempio superando la barriera ematoencefalica o ottimizzando il rilascio dei farmaci. Grazie ai progressi nella ricerca, la nanomedicina apre nuove prospettive per trattamenti personalizzati e più efficaci.
La nanomedicina nel trattamento oncologico
La nanomedicina applicata all’oncologia si basa sull’utilizzo di nanoparticelle per veicolare agenti terapeutici direttamente alle cellule tumorali. Queste particelle, grazie alle loro dimensioni ridotte (nell’ordine dei nanometri), riescono a penetrare in modo più efficiente nei tessuti e a superare le barriere biologiche che ostacolano l’assorbimento dei farmaci tradizionali. Questo permette un rilascio controllato e specifico dei principi attivi, aumentando la concentrazione del farmaco nel sito tumorale e minimizzando l’esposizione dei tessuti sani, riducendo così la tossicità sistemica. Un esempio pratico di questo approccio è l’uso di nanoparticelle lipidiche o polimeriche per incapsulare farmaci chemioterapici, consentendone un rilascio prolungato e mirato. Inoltre, alcune nanoparticelle possono essere progettate per rispondere a stimoli specifici, come il pH acido del microambiente tumorale, innescando la liberazione del farmaco solo nelle aree affette.
Nanofarmaci approvati e in sperimentazione clinica
Negli ultimi anni, diversi nanofarmaci sono stati approvati per la terapia del cancro, mentre altri sono attualmente in fase di sperimentazione clinica. Le formulazioni liposomiali, ad esempio, sono tra le più studiate e utilizzate in ambito oncologico. Un caso di successo è la doxorubicina liposomiale (Doxil), che ha dimostrato un’efficacia terapeutica superiore rispetto alla doxorubicina convenzionale, riducendo gli effetti collaterali cardiotossici. Oltre ai liposomi, altre tipologie di nanoparticelle stanno mostrando risultati promettenti, come le nanoparticelle di oro e le nanocapsule polimeriche. Queste possono trasportare più farmaci contemporaneamente o essere combinate con agenti diagnostici per monitorare la risposta al trattamento in tempo reale. Tuttavia, la complessità nella preparazione delle nanoparticelle e la necessità di approvazioni regolatorie approfondite rappresentano ancora sfide significative. Gli studi clinici devono dimostrare non solo l’efficacia terapeutica dei nanofarmaci, ma anche la loro sicurezza a lungo termine.
Personalizzazione del trattamento oncologico
Uno degli aspetti più innovativi della nanomedicina è la possibilità di sviluppare trattamenti oncologici personalizzati, adattati alle specifiche caratteristiche molecolari del tumore di ogni paziente. L’uso di biomarcatori tumorali e la combinazione con tecnologie di imaging avanzate permettono di ottimizzare la scelta della terapia e il monitoraggio della sua efficacia nel tempo. Ad esempio, nanoparticelle funzionalizzate con anticorpi specifici possono essere progettate per riconoscere e attaccare selettivamente cellule tumorali con particolari mutazioni genetiche. Questo approccio consente di ridurre la variabilità della risposta ai trattamenti e di aumentare il successo terapeutico.
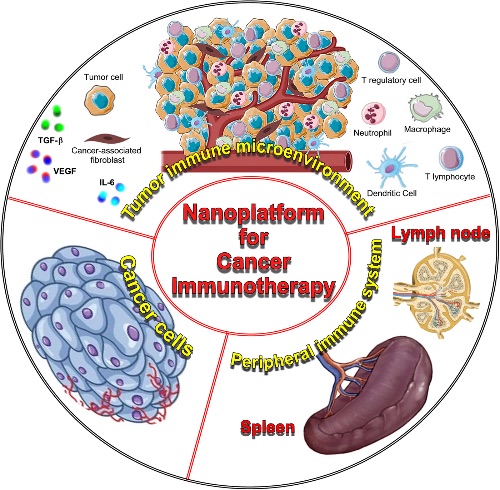
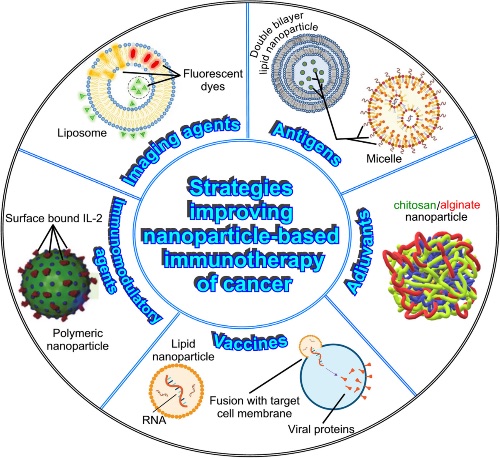
Nanoimmunoterapia
L’immunoterapia antitumorale abilitata al nano sta guadagnando attenzione come approccio innovativo per trattare i tumori. La nanoimmunoterapia si concentra sull’uso di nanoparticelle per potenziare la risposta immunitaria contro il tumore. Le nanoparticelle possono essere progettate per mirare alle cellule tumorali, innescando la morte cellulare immunogenica e il rilascio di antigeni tumorali e molecole associate al pericolo. Inoltre, le nanoparticelle possono intervenire sul microambiente tumorale, rieducando le cellule immunosoppressive, come i macrofagi M2 protumorigeni, i neutrofili N2 o le cellule T regolatorie, in modo da migliorare l’infiltrazione delle cellule killer e la risposta immunitaria. Un altro approccio è il miglioramento della presentazione dell’antigene tumorale alle cellule dendritiche, stimolando la proliferazione delle cellule T citotossiche e potenziando così l’immunità antitumorale.
Uso combinato di nanoimmunoterapia e CRISPR/Cas9
Recentemente, la combinazione della nanoimmunoterapia con la tecnologia CRISPR/Cas9 ha suscitato grande interesse. CRISPR/Cas9 consente l’editing genico mirato, e quando combinato con nanoparticelle, può migliorare l’efficacia della terapia. Le nanoparticelle possono essere utilizzate per veicolare il sistema CRISPR/Cas9 direttamente nel tumore, modificando il DNA delle cellule tumorali per renderle più suscettibili all’attacco da parte del sistema immunitario. Inoltre, CRISPR/Cas9 può essere utilizzato per modificare le cellule immunitarie, come le cellule T e i macrofagi, per renderle più efficaci nel riconoscere e distruggere le cellule tumorali. In questo modo, l’uso combinato di nanoimmunoterapia e CRISPR/Cas9 potrebbe portare a una risposta immunitaria più forte e mirata contro il cancro, aumentando l’efficacia della terapia e riducendo gli effetti collaterali.
Vantaggi della nanomedicina oncologica
La nanomedicina offre numerosi vantaggi nel trattamento del cancro, rivoluzionando l’approccio terapeutico grazie a strategie mirate ed efficaci. Uno dei principali benefici è il rilascio mirato del farmaco, che consente di ridurre la tossicità sistemica e aumentare l’efficacia terapeutica, minimizzando gli effetti collaterali sui tessuti sani. Inoltre, le nanoparticelle permettono il trasporto simultaneo di più farmaci, facilitando la combinazione di diverse terapie in un’unica somministrazione. Un altro aspetto è la possibilità di monitorare in tempo reale l’andamento del trattamento grazie all’uso di nanomateriali per l’imaging diagnostico, che permettono di visualizzare l’accumulo del farmaco nelle cellule tumorali e di valutare la risposta alla terapia. Infine, la ridotta dimensione delle nanoparticelle garantisce una maggiore penetrazione nei tessuti tumorali, superando le barriere biologiche che spesso ostacolano l’assorbimento dei farmaci convenzionali, aumentando così la loro efficacia terapeutica.
Conclusioni e prospettive future
Nonostante il grande potenziale della nanomedicina oncologica, esistono ancora diverse sfide da affrontare prima che queste tecnologie possano essere ampiamente integrate nella pratica clinica. La produzione delle nanoparticelle è complessa e costosa, richiede infrastrutture avanzate per la sintesi e caratterizzazione, il che ne limita l’accessibilità su larga scala. Inoltre, la regolamentazione dei nanomateriali risulta particolarmente stringente, poiché le agenzie preposte all’approvazione dei farmaci devono valutare con attenzione la loro sicurezza ed efficacia, rallentando i tempi di immissione sul mercato. Un’altra questione cruciale riguarda la sicurezza a lungo termine delle nanoparticelle, poiché al momento mancano dati sufficienti sugli effetti prolungati nell’organismo umano. Superare questi ostacoli richiederà ulteriori ricerche, investimenti e una stretta collaborazione tra scienziati, industrie farmaceutiche ed enti regolatori, con l’obiettivo di rendere la nanomedicina una realtà consolidata nel trattamento del cancro.